θ�����������ø���Լ�DNA����Ĺ�ϵ
��֢ 2000���1�ڵ�19�� �����о�
���ߣ����㡡����÷������ӡ�����ﰲ����ΰ�졡����ԡ�ׯ��
��λ�����㡡����÷������ӡ�����ﰲ����ΰ�졡����ԣ��ӱ�ҽ�ƴ�ѧ�����ڶ�ҽԺθ����ƣ��ӱ�ʯ��ׯ050000����ׯ�٣���ž�ʯ��ׯҽѧ�ߵ�ר��ѧУ���ӱ�ʯ��ׯ050000��
�ؼ��ʣ�θ������������ø���ۺ�ø����Ӧ����ʽϸ����
����ժ��Ҫ��Ŀ�ģ��о�θ���������ø������Լ�DNA����Ĺ�ϵ�������������ظ�������ø��������������TRAP��ELISA������������������ж�ճĤ����ø����,��ʽϸ�������������DNA���塣����������������ø������ռ84.0����42/50��,�����ж�ø������ռ2.0����1/50��������ø�����������챶������ռ52.38����22/42��,������ø�����������챶����֣�����ø��������ƽ��ֱ��6.5cm,��������ƽ��ֱ��3.9cm;����ø���������ܰ�ת����Ϊ59.5����25/42��,������ת����Ϊ12.5����1/8�������߲������������壬Pֵ�ֱ�Ϊ��P��0.005,P��0.05��P��0.002,P��0.05�����ۣ�θ����������ø��������,ø���������챶�巢���ʸߣ���������ܰ�ת���ʸߣ�˵������ø�ļ����ڶ��������ķ�����չ������Ҫ���أ������뼲���Ľ�����ء�
��������ţ�R735.2��R735.3�����ױ�ʶ�룺A
�������±�ţ�1000��467X(2000)01��0042��03
Telomerase activity and DNA ploidy in gastric cancer
����and colorectal cancer
ZHANG Yan, JIA Ru-mei, ZHANG Yu-yin, et al.
����(Second Hospital of Hebei Medical University,Shijiazhuang 050000�� P.R.China )
����Abstract:Objectives��To study the relation between telomerase activity or DNA ploridy and progression of gastric cancer and colorectal cancer.Methods��Telomerase activity was detected using telomeric repeat amplification protocal-enzyme linked immunosorbent assay(TRAP-ELISA). The DNA content was detected using flow cytometry.Results��Most of the carcinomas (42/50) were telomerase positive, but the telomerase activity was observed infrequently in adjacent mucosa (1/50) (P��0.005). In this study, the aneuploid carcinomas were 52.38�� (22/42) in telomerase-positive group, but there were no aneuploid carcinoma in telomerase-negative gronp, (P�� 0.05). The mean diameter of telomerase-positive carcinomas was 6.5 cm, but the diameter of telomerase-negative carcinomas was 3.9 cm (P�� 0.002). The percentage of lymph node metastasis in telomerase-positive carcinomas (25/42) was higher than that in telomerase-negative carcinomas (1/8), P�� 0.05.Conclusions��Telomerase is important in the carcinogenesis of gastric cancer and colorectal cancer, and it is correlated with the progression of the diseases.
����Key words�� Gastric cancer; Colorectal cancer; Telomerase; Polymerase chain reaction; Flow cytometry ��
�����������Զ��������������Ƶ��о�Խ��Խ���룬����Ⱦɫ��Ļ��䡢ԭ������ļ���ְ������ͻ�����������ϵ�������о�����θ�������ķ��������ø�����ϵ���У���ʾ����ø�������������ķ�������չ������Ҫ���á�
����1�����뷽��
����1.1����
������ʵ�鹲ȡ�걾50����Ϊ1998��2�¡�1998��9�¾����ںӱ�ҽ������Ժ�IJ���������θ��30��������40��71�꣬�С�ŮΪ22��8����20��������24��70�ꡣ�С�ŮΪ12��8�����в�����������֤ʵΪ���������������ơ������г��걾������ȡ�ģ�Ͷ����С����ڶ���ø���ı걾��Сʱ�����ڣ�80����䱣�棻����DNA��������ı걾��70���ƾ��̶���4����䱣�档��ȡ�걾����һ�����ڼ�⡣���ڶ���ø�����Լ�Ϊ�¹���������˾Telomerase PCRELISA�Լ����ṩ��PCRѭ����Ϊ����PE��˾��Ʒ���ͺ�480����ʽϸ����ΪB.D��˾FACSCalibur��
����1.2����
����1.2.1����ø��⣺����TRAP��ELISA���������岽�����£�ȡ2mm3�걾���ѽ�Һ60��l�����飬0�澲��30���Ӻ���15000prm4������20���ӣ�ȡ����Һ5��l������ֹ��ȷ��ⶨ������Լ50��g����PCRѭ�������25��l����������Ϊbiotin��ǣ�����ˮ20��l����PCR������ѭ��1��10min��25�棻ѭ��2��5min��94�棻ѭ��3��32��30s94�棬30s50�棬90s72�棻ѭ��33��10min��72�档PCRѭ������5��l������Һ20��l���ȣ����·���10min�����ӽ�Һ225��l���ӽ�̽��ΪDIG��ǣ���ȡ�����100��l����MTP�壨�Ѱ���biotin���壩���¾���2Сʱ��ϴ����뿹DIG-POD�������¾���30���ӣ�ϴ�壬�ټ���POD����100��l����Ӧ15���Ӽ���ֹҺ����30��������ø���Ƕ�ȡ�����ֵ��OD������450nmΪ��Ⲩ����960nmΪ�ο�����������OD��0.200Ϊ���ԣ�0.200��OD��0.500Ϊ����0.500��OD��1.000Ϊ������OD��1.000Ϊ��������
����1.2.2DNA�����⣺��5mm3�걾��120Ŀ������������ĥ��ϸ����Һ��100ת/�ֳ�������5����������Һ������0.5��θ����ø2ml37������30���ӣ�300Ŀ���������ˣ�1000ת/������5���Ӻ������壬����70���ƾ�3ml��4������ҹ������Bio-Rad��˾�ṩ��DNA INDEX AND CELL CYCLE EVALUATION�Լ��У���һ��������DNA����ļ�⣬DNAָ����DI����0.9��1.1��Ϊ�����壬���ڴ˷�Χ��Ϊ�챶�塣
����1.2.3ͳ��ѧ�������ֱ���æ�2���飬t������Ⱥͼ��飬����ͳ��ѧ���������������
����2���
����θ��������Ϊ������������������ֳ������,���������Ķ���ø������Ϊ84.0������������Ϊ13����������Ϊ10��������Ϊ19���������ж�������Ϊ2.0������Ϊ�����ԣ����弰�ж˵����������������죬P��0.005������1����˵������ø��������������������һ���ձ�����
��1�����弰�����ж˶���ø���ԱȽ�
| ��λ |
������� |
����(%) |
����(%) |
| ���� |
50 |
8(16.0) |
42(84.0) |
| �ж� |
50 |
49(98.0) |
1(2.0) |
����ͳ��ѧ����������У����2����P��0.05��������ø���Լ������ٴ������Ĺ�ϵ����2��ø�����벡�������䡢�Ա������Ĵ�����ͺͲ��������أ��������С���ܰ�ת��Ӱ����ø���ԡ�����ø���Ե�����ƽ��ֱ��Ϊ6.5cm����ø���Ե�����ƽ��ֱ��3.9cmΪ��P��0.002��������ø���������ܰ�ת����Ϊ59.5�������Ը��ڶ���ø���ԣ�12.5������������P��0.05����
��2������ø�����������ٴ������Ĺ�ϵ
| �ٴ����� |
���� |
���� |
Pֵ |
| 1ƽ������ |
54.00��10.52 |
56.66��9.43 |
��0.05 |
| 2�Ա�(��:Ů) |
5:3 |
29:13 |
��0.05 |
| 3����ƽ��ֱ��(cm) |
3.9��1.4 |
6.5��2.4 |
��0.002 |
| 4�ܰ�ת��(��) |
1 |
25 |
��0.05 |
| 5�������(��) |
�� |
| ������ |
7 |
33 |
��0.05 |
| ������ |
1 |
6 |
| ���� |
0 |
3 |
| 6��֯ѧ����(��) |
�� |
| �ٰ� |
5 |
19 |
��0.05 |
| ճҺ�ٰ� |
1 |
11 |
| �ͷֻ��� |
2 |
12 |
����ͳ��ѧ������1��3�����t���������2��4�����У����2
�������飻5��6�����Ⱥͼ������̬���Ʒ�����ͬʱ��������ʽϸ�����ⶨ�˱걾��DNA����������3��������ø���������챶��ռ52.38���������߾�Ϊ�����壬����ø���������챶������������ߣ�P��0.05)����ʽϸ�����ⶨDNA�걾���壬�����ͼ1��5��
��3������ø������ϸ��DNA�����ϵ
| ��Ӧ |
������� |
�챶�� |
������ |
| ���� |
42 |
22 |
20 |
| ���� |
8 |
0 |
8 |
����ͳ��ѧ���������æ�2����P��0.005
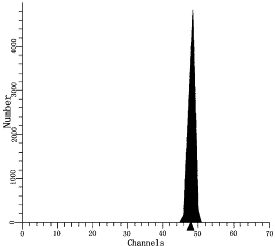
ͼ1������ѪDNA����ͼ
����DI=1.00��S=0.00����CV=1.44
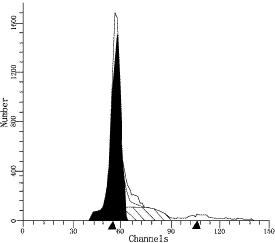
ͼ2θ���걾DNA����ͼ�������壩
����DI=1.07��S=25.85����CV=4.57
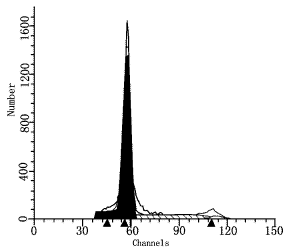
ͼ3�᳦���걾DNA����ͼ�������壩
����DI=1.08��S=18.13����CV=4.03
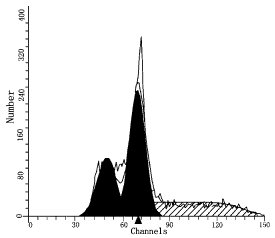
ͼ4θ���걾DNA����ͼ���챶�壩
����������壺DI=0.98��S=0.00����CV=11.74
�����챶��壺DI=1.38��S=37.68����CV=7.62
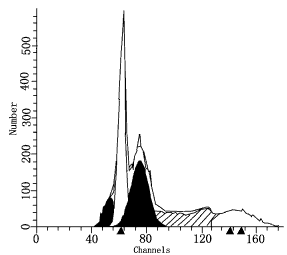
ͼ5ֱ�����걾DNA����ͼ���챶�壩
������������DI=1.03��S=0.00����CV=7.42
�����챶���1��DI=1.24��S=43.58����CV=4.13
�����챶���2��DI=1.50��S=0.00����CV=8.31
����3����
����������Ⱦɫ��ĩ�˵�һ���������У���DNA�������������1���������Ĵ���ʹȾɫ��ĩ�˱����ȶ�������DNA�ۺ�ø���ܸ��ƶ�������������ϸ�����Ѷ����̣������̵�һ���̶Ⱥ�ϸ����������ϸ���д���һ�������ø��������ø���ӳ�������2����ʹϸ����Ϊ������ϸ����������ϸ���ж���ø���ԣ�������˿���Ѵ��������ӣ����������̣�ϸ���Ⱥ���M1�ڡ�M2�ں����ڶ����������̣�Ⱦɫ����ָ����쳣��̬������ϸ����������������ϸ�������˶���ø�������������̣���Ϊ������ϸ������������������ġ�����������øѧ˵����3����Monika����4������������᳦ճĤ50�����᳦��10�����᳦����20�����᳦��50��������ø�����ʷֱ�Ϊ0����40����60����90����Hiyama����5�����66��θ�����ж˶���ø���ԣ�����θ����������Ϊ82��(14/17)��������������Ϊ86��(42/49)���ж�������Ϊ6��(4/66)���Ҷ���ø���Ե�����������ܰ�ת���ʸߡ�Ԥ����ʵ����θ������ø������Ϊ83.3������Ϊ85���������ж�������Ϊ2.0����ͬʱ���ǵļ��Ҳ����������ø�����벡�����䡢�Ա������Ĵ��弰���������أ���������Ĵ�С���ܰ�ת���������Թ�ϵ�����������ױ��������������Щ�о������ʾ������ø����������θ���ʹ�����һ���ձ������ҿ����ڰ�ǰ������֯�м������Ų���Ľ�չ�����������ߣ��뼲��������ء�����ø�����������ܰ�ת�������ߣ��������������ѧ��Ϊ��������ϵ������ø������Ϊθ����������ϵ�������־�
������������Ƿ���һ��θ���ж�Ϊ����ø���ԣ��������ΪճĤ�ض���֢�鲻���������������ж�ø���Ե�ԭ��Ϊ����1���ж���֯�ض���֢�������ܰ�ϸ�������ܰ�ϸ�������Ķ���ø������6����������֢��Ӧ���ص���֯���ܶ���ø��������ԣ���2���ж���֯��ת�������£�������������ͨ���⾵���һ��ƽ�����ް�ת�ƣ�����ø������Dzⶨ�����ſ�ϸ����ø���ԣ��ȹ⾵��ȫ�棬����������ת�����3����ǰ����Ҳ�ɵ��¶���ø���Ա�����7�����òж����ԵIJ���Ϊ�ضȳ���Ƥ�������ɵ��¶���ø���Ա��
�����ڶ���ø��������У����������̣���������Ҫ����֮һ��ά��Ⱦɫ����ȶ��ԣ���ֹȾɫ����ںϼ����⡣���������̵�һ���̶ȶ�����ά���书�ܣ�Ⱦɫ��ͻᷢ�����䣬�γ�˫��˿��Ⱦɫ�塢����Ⱦɫ�弰Ⱦɫ��ȱʧ����8������ʱϸ�������Ϊ�챶�塣ͬʱ��Щ���̵Ķ���Ҳ�ἤ�����ø�����Զ���ø���Ե�ϸ���챶������ϸߡ���ʵ����ø�������챶��ռ52.4���������������챶����֡��ձ�ѧ��Okusa����9�����о�������������ƣ���Ϊ�챶�������Ķ���ø���Ը����������������챶������Ⱦɫ�巢�����䣬���Գ̶ȸߣ�ת���ʸߣ�Ԥ�����������ø���Կ��Է�Ӧ�����Ķ���DZ�ܣ��벡��Ԥ����ء�
������֮��θ����������ø�������ߣ�����ø����������������������ܰ�ת���ʸߡ��챶�庬���ߡ�Ԥ��������Щ���������������ø�����ڶ�����������������Ҫ���أ�����ø����Ϊ�ٴ�����Ԥ���ж��ṩ������Ϣ��
����������Ŀ���������ܺӱ�ʡ����������(98002��)����
������ͨѶ���ߣ�Tel��86��311��7046901��6831
����E��mail��meaky��zdgm@163.net
�����ο����ף�
����[1]M ller HJ. The remarking of chromosomes [J]. Woods Hole,1938,13�� 181.
ller HJ. The remarking of chromosomes [J]. Woods Hole,1938,13�� 181.
����[2]Greider CW, Blackburn EH. Identification of a specific telomere terminal transferase activity in Tetrahymena extracts [J]. Cell,1985,43�� 405�� 413.
����[3]Rhyu MS. Telomeres, telomerase and immortality [J]. J Natl Cancer Inst,1995,87�� 884�� 894.
����[4]Engelhardt M,Drullinsky P, Guillem J, et al.Telomerase and telomere length in the development and progression of premalignant lesion to colorectal cancer [J]. Clin Cancer Res,1997,3�� 1931�� 1941.
����[5]Hiyama E, Yokoyama T, Tatsumoto N,et al. Telomerase activity in gastric cancer [J]. Cancer Res,1995,55�� 3258�� 3262.
����[6]Hiyama K, Hirai YK, Kyoizumi SS, et al. Activation of telomerase in human lymphocytes and hematopoietic progenitor cell [J]. Jimmunol, 1995,155�� 3711�� 3715.
����[7]Yashima K, Litzky LA, Kaiser L, et al. Telomerase expression in respiratory epithelium during the multistage pathogenesis of lung carcinoma [J]. Cancer Res, 1997,57�� 2373.
����[8] Blackbur n EH. Structure and function of telomeres [J]. Nature,1991,350�� 569.
�ո����ڣ�1999��03��16
�����ڣ�1999��04��23