在正常情况下,人体血浆pH值平均为7.4,变动范围很小(pH7.35~7.45)。而机体每日代谢产酸量是很大的,例如,非挥发酸可达50~100毫克当量,CO2可达400升。这些酸性物质必须及时处理,否则血浆pH值不能保持正常。这就靠一整套调节机构密切协同来完成。
血液中有一系列缓冲物质。根据化学上的缓冲作用原理,我们人为地把它们归纳为四个主要的缓冲对,即NaHCO3/H2CO3,Na2HPO4/NaH2PO4,B·血浆蛋白/H·血浆蛋白,B·Hb/H·Hb。它们具有很强且很迅速的缓冲酸碱度改变的能力。例如,我们将10mmol(毫克分子)的HC1加1000毫升中性蒸馏水中,其pH值可从7降至2,但同量酸加于1000毫升血浆中,其pH值的变化却很小,以致一般几乎测不出来。
每一对缓冲物质既能缓冲酯也能缓冲碱,其中以NaHCO3/H2CO3这一对最为重要,因为它的量最大。它对酸的缓冲区反应如下:
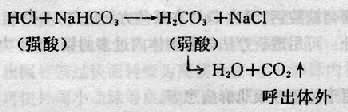
从上面的反应可以看出,经NaHCO3缓冲,解离度大的强酸HC1转变为解离度小的弱酸H2CO3,后者在体液中的解离度仅约为前者的1/1500。因此使[H+]大为减小。而且H2CO3还能分解为H2O和CO2,CO2又能呼出体外。医学实践中将血浆中NaHCO3称为碱贮备,以二氧化碳结合力表示之。正常值为27mmol(或毫克当量)/升或60容积%。
这也是缓冲方式之一。当能改变酸碱平衡的离子如H+、HCO3-等在细胞外液中升高时,它们能进入细胞内(或进入骨内)换出与其符号相同的离子,以保持细胞外液之pH值。其变化可简单表示如下:
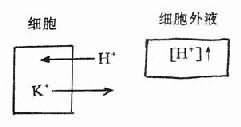
进入细胞内的H+可与细胞内的化学缓冲物质起化学反应而被缓冲。根据实验研究估算,酸或碱在细胞外液增加后,一般约经2~4小时,将有1/2的量进入细胞内。所以尽管细胞内液量大于细胞外液量一倍,但二者化学缓冲总能力却大致相等,可见细胞外液中缓冲物质的浓度是高于细胞内液的。
这个事实对治疗有关。举一代谢性酸中毒病人用NaHCO3治疗时的情况为例:
病人体重=60公斤
细胞外液量=0.20×60=12升
治疗前血浆[HCO3-]=13mmo1(或毫克当量)/升
给NaHCO3量=100mmo1

病人治疗后实测血浆[HCO3-]=16.7mmol/升
实践证明,上述规律是较为可靠的。因此在纠正酸碱中毒时应考虑离子转移这一变化。计算输液量时要将这一变化估计在内。
呼吸调节(一般10~30分钟即可将轻度的一次性变动代偿过来)。[H+]增高和[CO2]增高,均能剌激呼吸中枢;H+还对颈动脉体和主动脉体的化学感受器起刺激作用,这都可引起呼吸加深加快,使CO2排出增加。从上面介绍的缓冲反应来看,每排出一个CO2分子,也就等于清除了一个H+离子,如:
H++HCO3-→+H2CO→H2C+CO2↑(增多) 碱贮 (呼出)
肾脏调节(数小时至数日完成):肾脏是酸碱平衡调节的最终保证。因为只有CO2可以通过呼吸排出体外(CO2即可代表可挥发酸H2CO3,因为CO2+H2O→H2CO3),而其它如乳酸、丙酮酸、β-羟丁酸、乙酰乙酸、硫酸、磷酸、尿酸、草酸等均为非挥发酸,最终均需通过肾脏把前面三项调节所造成的变动调整过来。把过多的排出,把不足的保留下来。因此肾脏调节机体酸碱平衡的功能正常与否,关系重大。
肾脏排酸有三种形式:
(一)自由H+:虽然它决定着尿液pH值,但是其量却很少(每日只1~2毫克当量)。尿pH为5时,[H+]为0.00001克分子,pH为8时,[H+]为0.0000000克分子。尽管它确是一种存在形式,它只是尿中大量酸性物质的一个很小部分。而肾脏排酸主要是以下二种形式。
(二)NH4-:是H+与NH3作用形成的。NH3由肾小管产生,在体内是很强的碱性物,与H+的亲和力极大。它弥散至尿中与H+结合。示意如下:
人体每日由代射所产生的非挥发酸总量约50~100mmol,其中一半以上(1/2~2/3)是以此种形式排出的。
(三)可滴定酸:是由H+与缓冲物质(主要是HPO4=作用形成的。用NaOH把尿滴定至与血浆相同之pH,即可测知可滴定酸量。可滴定酸的形式约占肾排酸总量的少一半(1/3~1/2)。
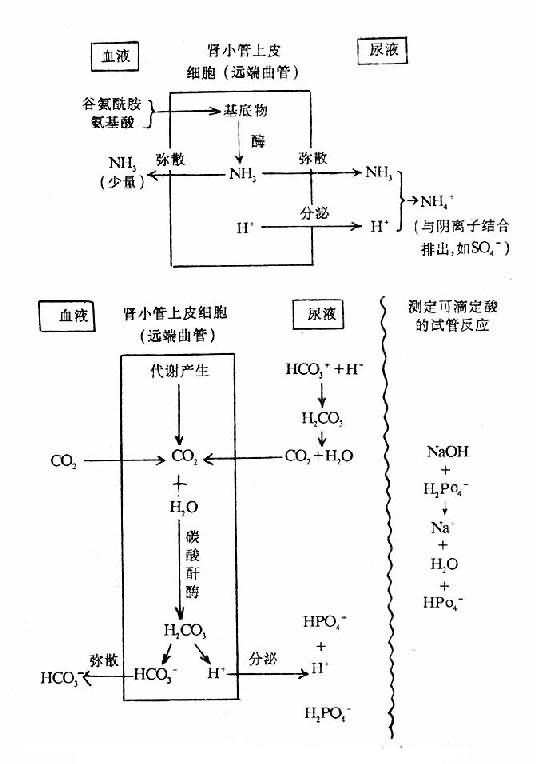
肾小管上皮细胞分泌的H+,在近曲小管几乎全部用于重吸收HCO3-;在远曲小管则几乎全部用于生成可滴定酸和NH4+。这与肾脏疾病的代谢性酸中毒如肾小管性酸中毒的关系密切。可滴定酸的形成示意如下:
| Copyright @ 2002-2010 婵炴垶鎼╅崢鑲╀焊閻楀牏鈻旀い鎾偓宕囥偐缂備礁顦拌摫闁哄瞼鍠撶槐鏃堟晸閿燂拷. xxmy.com 闂佺粯顨呴悧濠傖缚閸儱绠ラ柍褜鍓熷鐢告晸閿燂拷 濠电姭鍋撴俊銈囨嚕P婵犮垼顔愰幏锟�10017704闂佸憡鐟遍幏锟� |